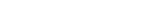
Blanco para Zika
Un equipo internacional, con participación de científicas y científicos argentinos, detectó una proteína celular que ayuda a propagarse al virus del Zika, causante de malformaciones en recién nacidos. Pero no solo la identificó sino que la neutralizó y avanzó con un tratamiento que logró contrarrestar daños de la enfermedad. Por ahora, las pruebas son en un modelo animal pero podría servir para terapias en mujeres embarazadas.
María creyó que con el parto habían acabado los dolores. Pero, enfrentaba uno mayor: su hijo recién nacido, mostraba una cabecita más chica que lo normal, y podría tener problemas para caminar, oír o ver. Era un bebé Zika. En algún momento de su embarazo, algún mosquito del género Aedes, infectado, la picó y le transmitió el virus ZIKV, que fue aislado por primera vez en 1947 en el bosque de Zika, en Uganda. Desde entonces, los casos pasaban inadvertidos en África y algo en Asia, hasta que desembarcó en América hace unos seis años pero con distintas consecuencias.
Ahora, la ciencia, desde Brasil, Estados Unidos y Argentina, acaba de aplicar un tratamiento promisorio en un modelo animal, y que -de superarse todas las pruebas- podría ser usado en mujeres embarazadas. Asimismo, este hallazgo abre expectativas a posibles desarrollos de antivirales de amplio espectro que sirvan, además del Zika, para contrarrestar infecciones como dengue, fiebre hemorrágica argentina y COVID-19.
Fiebre leve, erupción, conjuntivitis, dolor muscular, articular o de cabeza son algunos de los síntomas visibles de Zika, pero ¿qué ocurre en el interior del cuerpo cuando acecha el virus? ¿Este patógeno encuentra en la célula algún elemento que lo ayuda a propagarse? El equipo local e internacional detectó a un aliado celular, lo neutralizó y diseñó un tratamiento en pruebas de laboratorio con ratones. Los resultados mostraron que la terapia “limitó la replicación del ZIKV y mejoró la microcefalia del recién nacido en un modelo murino», indica la investigación publicada en Nature Neuroscience.
El trabajo de cooperación internacional contó con numerosos argentinos como participantes. Algunos de ellos son Federico Giovannoni -como primer autor-, Elsa Damonte, María Torti, Cybele García y Francisco Quintana. Estos dos últimos, investigadora e investigador responsables, junto con Jean Pierre Schatzmann Peron, de la Universidad de São Paulo, Brasil.
Primeros pasos
La mirada científica apuntó con intensidad hacia ZIKV, luego de que un primer brote de casos afectó el noreste de Brasil, poco después del Mundial de Fútbol de 2014. Y un año más tarde, hubo un alarmante número de recién nacidos con microcefalia.
Mientras la inquietud crecía, estas investigaciones buscaban proteínas celulares que pudieran ayudar al virus a replicarse. “Una de ellas, el factor AHR, era estudiado por Quintana, nuestro colega argentino en el Brigham and Women´s Hospital de la Universidad de Harvard, en Boston, en el contexto de la esclerosis múltiple, una enfermedad que afecta al sistema nervioso central, al igual que el Zika. Entonces, decidimos sumar esfuerzos”, narra Cybele García, del Laboratorio de Estrategias Antivirales de la Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires.
AHR, sigla en inglés del receptor de hidrocarburos de arilo, resultó ser un factor cada vez más sospechoso en este trabajo detectivesco de la ciencia. Distintos registros daban cuenta de que esta molécula estaba exacerbada en los perfiles genéticos de las personas infectadas de Zika. Además, tras revisar numerosas bases públicas de datos “encontramos que en la placenta de mujeres embarazadas, AHR estaba muy sobreexpresado. Nos dedicamos a este factor al que, hasta entonces, nadie le había prestado mucha atención”, agrega.
Apunten a AHR
En el mundo microscópico celular, aparentes pequeñas decisiones pueden generar temerarias consecuencias. En este caso, tras diversos experimentos, los estudios mostraron que AHR ya no era sospechoso, sino responsable de ayudar al virus a propagarse en el cuerpo. De este modo, por primera vez, se había identificado este mecanismo, por el cual, esa molécula presente en las células hospedadoras era aprovechada por Zika para replicarse más exitosamente.
Todos estos microacontecimientos tampoco parecen estar ajenos a los problemas de medio ambiente. “AHR es un sensor de polución, que se activa y dispara cuando estamos inmersos en contaminación ambiental del aire, agua, o de lo que consumimos. Este factor, ahora sabemos que, al incrementarse -precisa García- ayuda a la virulencia del Zika”.
En este aspecto, ella comenta que un caso muy estudiado fue en Recife, Brasil, una de las sedes del Mundial FIFA 2014. “Este evento atrajo a numerosos viajeros en un sitio de muchos mosquitos, con agua contaminada por cianobacterias que producen una toxina, candidata a activar AHR. Doce meses después, hubo una explosión de recién nacidos con microcefalia, unas veinte veces por encima de lo habitual. Nosotros, suponemos que el componente ambiental colaboró en este brote en esa zona”, sugiere, y enseguida subraya: “Una persona que vive en un contexto de ambientes degradados está más vulnerable a la infección por Zika. Por lo tanto, el desarrollo de su bebé tiene perspectivas más graves que el de quienes habitan un ambiente fuera de la polución”.
Pruebas con animales
Volviendo a la etapa inicial de este estudio, una vez identificado el mecanismo de cómo AHR ayuda a la replicación del virus de Zika, el paso siguiente consistía en neutralizarlo. Es decir, impedir la exacerbación de esta molécula y así controlar la multiplicación del ZIKV. Probaron diversos compuestos en el laboratorio, y evaluaron que estaban listos para iniciar otra etapa de la investigación.
“Decidimos que valía la pena realizar el desarrollo terapéutico en un modelo animal. Esto lo hicimos con Schatzmann Peron, un investigador muy importante quien junto con su equipo estableció la relación entre la infección del virus Zika y la microcefalia en los bebés”, precisa.
Ya en esta fase, echaron mano a dos drogas como terapia: una de uso comercial, y otra que está en vías de emplearse como medicamento contra el cáncer. “En ambos casos, los animales mejoraron. El parámetro de medición de cráneo, su masa encefálica y su peso dan casi como el de un ratón sano o normal. Eso nos dio la pauta de que el tratamiento que estábamos proponiendo era realmente muy bueno”, indica.
Por cierto, aún faltan numerosas pruebas antes de ser probado en embarazadas como tratamiento para contrarrestar las malformaciones del recién nacido, pero García remarca otro aspecto de estos estudios. “Estamos proponiendo una terapia contra una proteína celular que nosotros sabemos que es muy importante para otras infecciones virales como SARS-CoV-2 (causante de COVID-19), dengue o Junín (de fiebre hemorrágica argentina). Estas infecciones utilizan el mismo mecanismo de replicación que el Zika. El tratamiento podría funcionar como un antiviral de amplio espectro”, concluye.