Mejores que el original
Un equipo de científicas y científicos argentinos desarrollan en laboratorio compuestos similares a derivados del colesterol con una actividad distinta de la conocida. Esas modificaciones le otorgarían propiedades para combatir enfermedades y consiguen que no sean rechazados por el organismo.
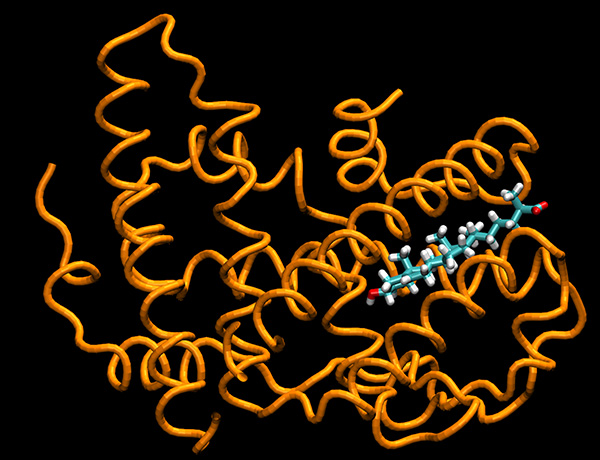
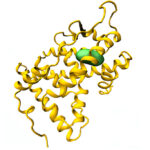
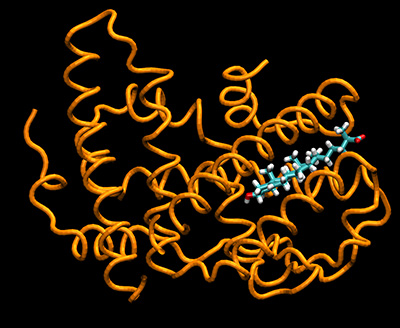
Las simulaciones por modelado molecular ayudaron a comprender cómo funcionan los nuevos análogos de un derivado del colesterol estudiados por los investigadores.
Las apariencias engañan. Y de eso se trata. ¿Cómo lograr elaborar artificialmente compuestos químicos, similares a los que poseemos en nuestro cuerpo, pero distintos? Apenas unos pequeños cambios que le aporten propiedades farmacológicas de modo de combatir enfermedades y, a la vez, que no sean rechazados por el organismo. Expertos en laboratorios de la Argentina diseñan, prueban, y buscan a diario llevar adelante este cometido, y obtienen resultados alentadores con estas imitaciones o análogos.
“Descubrimos nuevos análogos de oxiesteroles, un derivado del colesterol, con una actividad distinta de la conocida y eso podría resultar en posibles candidatos a drogas orientadas a combatir enfermedades metabólicas, Alzheimer, e incluso cáncer”, sintetiza el doctor en Química, Lautaro Álvarez, desde la Facultad de Ciencias Exactas y Naturales de la Universidad de Buenos Aires sobre un trabajo realizado bajo la dirección de Gerardo Burton, y recientemente publicado en The Journal of Steroid Biochemistry and Molecular Biology. (Ver recuadro)
Desde hace unos años, el equipo apunta su mirada al llamado receptor X de hígado, conocido por su sigla en inglés LXR (Liver X Receptors), que se descubrió hace unos veinte años y hoy es casi una estrella por el interés que despierta en el mundo académico. Al principio, se creía que sólo estaba en el órgano hepático y regulaba únicamente el transporte de colesterol, esta sustancia grasa necesaria para formar los ácidos biliares u hormonas, pero que, cuando sobrepasa los límites normales, es un factor de riesgo cardíaco, entre otros trastornos.
“Ahora sabemos que LXR está en casi todos los tejidos del organismo e implicado en cáncer, en problemas metabólicos, en Alzheimer”, detalla Álvarez, al tiempo que Virginia Dansey agrega: “LXR es un receptor nuclear, una de las proteínas predilectas de la farmacología, porque es drogable, es decir, cuando le coloco una molécula chiquita, puedo cambiar su función e inducir, por ejemplo, al control del colesterol, o cualquier patología en la que interviene”.
En acción
Sentado frente al monitor, Álvarez hace combinaciones posibles en su computadora para diseñar estos compuestos parecidos a los naturales pero con esas pequeñas diferencias que harían el cambio saludable. “Con un programa de computación, simulo qué pasaría en el receptor LXR si a estos análogos se les introducen distintas variaciones estructurales”, describe. En base a los resultados obtenidos, él propone al grupo de investigación qué probar para contar con más posibilidades de funcionar.
“Mientras el equipo hace las pruebas biológicas, yo voy simulando. O al revés”, precisa para indicar que el trabajo es de retroalimentación constante. En este ida y vuelta compartido del grupo, se decidió apuntar a una “partecita final de la estructura del colesterol, la cual interactúa con LXR y mueve el interruptor dando orden de encendido o apagado a determinada actividad celular”, explican.
Tras numerosas investigaciones, se diseñaron seis compuestos o análogos de oxiesteroles con mínimas variaciones en relación con los naturales. “Expandimos el universo químico natural de los oxiesteroles”, es como Dansey define a esos cambios que se le efectúan molecularmente para lograr modular la respuesta con fines terapéuticos. “De los seis, observamos que tres resultan activos en el receptor y son agonistas inversos, es decir que cuando agrego la droga, LXR es menos activo que cuando no la tenía”, indica.
Por ejemplo, estos nuevos análogos podrían inducir a este estratégico receptor a modular respuestas que reviertan patologías. “Nuestra idea es diseñar compuestos que regulen LXR, observar cómo afectan la estructura del receptor y después estudiar su aplicación para cáncer de mama en una investigación dirigida por Adalí Pecci”, acota Dansey.
Por ahora, la línea de trabajo está en sus primeras fases, en la etapa de investigación básica con líneas celulares. “La farmacología –subraya Álvarez- busca descubrir nuevas moléculas que tengan nuevos efectos. En general, apuntamos a desarrollar posibles candidatos a nuevas drogas, pero eso puede llevar muchos años y requiere mucha inversión. Al mismo tiempo, al tener estas moléculas entendemos cómo actúa este receptor LXR, esto genera todo un conocimiento sobre su modo de acción que puede ser aprovechado por otros grupos científicos de aquí y del mundo”.
En detalle
La investigación publicada recientemente en The Journal of Steroid Biochemistry and Molecular Biology fue realizada por Lautaro Álvarez, Virginia Dansey, María Florencia Ogara, Carina Inés Peña, Rene Houtman, Adriana Veleiro, Adalí Pecci y Gerardo Burton de los departamentos de Química Orgánica y Química Biológica de la Facultad de Ciencias Exactas y Naturales de la UBA, UMYMFOR (UBA – CONICET), IFIBYNE (UBA – CONICET), y PamGene International, de los Países Bajos.