Desenmascarando proteínas
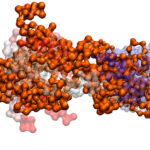
Las proteínas constituyen verdaderas nanomáquinas que hacen posible las realidades químicas que nos constituyen e identifican como seres vivos. Para averiguar cómo funcionan las proteínas, los investigadores construyen modelos que describan e integren aspectos del funcionamiento general de las proteínas y los aplican a sistemas experimentales.
Las proteínas son tan importantes que intervienen prácticamente en todas las funciones biológicas de cualquier organismo vivo.
En el Laboratorio de Fisiología de Proteínas, un equipo de especialistas iniciado por los doctores Ignacio Sánchez y Diego Ferreiro se dedica a desentrañar las interacciones de las proteínas con su entorno.
“La pregunta más general que atañe a nuestra especialidad es: ¿cómo funcionan las proteínas? Esta pregunta es tan abarcadora que resulta más útil para contemplarla que para responderla, pues las proteínas hacen de todo”, sintetiza Ferreiro. “Las proteínas son polímeros de aminoácidos que tienen un comportamiento fisicoquímico muy extraño, pues la mayoría de los polímeros no hacen nada. Las proteínas se pliegan, se mueven, se arman, se desarman, se pegan, se despegan, reconocen, mutan, catalizan, transforman, integran, procesan y distribuyen información, formando verdaderas nano-máquinas que hacen posible las realidades químicas que nos constituyen e identifican como seres vivos. Ante esta amplitud de comportamientos, las preguntas formuladas tienen que ser muy concretas. Para esto construimos modelos que describan e integren aspectos del funcionamiento general de las proteínas y los aplicamos a sistemas experimentalmente accesibles”, relata, con entusiasmo, el investigador.
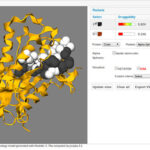
El equipo de científicos desarrolla herramientas teóricas, computacionales y experimentales para analizar diferentes aspectos del funcionamiento de proteínas y las aplican en sistemas modelo. “Tratamos de falsificar teorías con experimentos (de mesada y en computadora) y si una teoría se la banca, le seguimos tirando con bala”, grafica Sánchez.
”Como modelo de emergencia de una actividad catalítica estudiamos las lactamasas, enzimas que degradan antibióticos beta-lactámicos. Hay mucha información sobre estas proteínas de obvia importancia médico-sanitaria, pero poco entendimiento profundo de cómo los cambios en la secuencia de aminoácidos y en el microentorno afectan el plegado, la dinámica y la función proteica. Esto impide que podamos diseñar racionalmente inhibidores efectivos, ingenierear enzimas para que catalicen una reacción arbitraria deseada y predecir cambios evolutivos, por dar algunos ejemplos”, agrega Ferreiro.
Los investigadores utilizan como modelo de proteínas que reconocen y se pegan a otras macromoléculas al factor de transcripción E2 del virus del papiloma humano (HPV) y las proteínas repetitivas. La primera es una proteína que tiene la capacidad de reconocer secuencias de nucleótidos en ADN no específico de un genoma, con altísima especificidad y afinidad en apenas milisegundos. “¿Cómo pueden las proteínas discriminar sitios en una molécula que es estructuralmente regular, poco reactiva y tan químicamente aburrida como el ADN?”, se pregunta -no sin cierto humor- Sánchez.
Las proteínas repetitivas se forman con repeticiones en tándem de motivos de secuencia similares. “Son casos curiosos donde las simetrías internas permiten simplificar la descripción del paisaje energético de plegado, facilitando el mapeo entre las secuencias y las formas estructurales. Para ejercer una acción biológica, las proteínas tienen que poder moverse, desplegarse, visitar varias estructuras. Las proteínas tienen entonces que ser suficientemente estables para plegarse, a la vez que necesariamente inestables para moverse”, explica Ferreiro. Los investigadores buscan saber si existen conflictos que frustren las configuraciones, cómo podría impactar esto en la función y hasta qué punto es válida la teoría de los paisajes energéticos de plegado. “Este es el tipo de preguntas que le hacemos a las proteínas repetitivas”, agrega.
“Estudiamos también regiones proteicas naturalmente desplegadas que contienen pequeñas palabras que son reconocidas específicamente por otras proteínas. Aplicamos la teoría de la información molecular para descomponer los contribuyentes energéticos de la afinidad y especificidad de esta lectura. Los patrones derivados los usamos para inferir el comportamiento biofísico de regiones similares en la escala de los genomas enteros. Nos centramos en las interacciones virus-huésped, pues éstos tienen una limitación intrínseca en la capacidad de almacenar información genética y utilizan frecuentemente estas palabras”, completa Sánchez.
Los investigadores del Laboratorio de Fisiología de Proteínas son miembros también de la Asociación Argentina de Bioinformática y Biología Computacional, una asociación que promueve el desarrollo de la investigación en biología utilizando herramientas informáticas. La Asociación reúne a profesionales de distintas ramas de la biología, la matemática y la computación con el objeto de avanzar en el conocimiento de los seres vivos y en el desarrollo de aplicaciones productivas mediante métodos computacionales. Desde allí, Sánchez, Ferreiro y su gente trabajan fuertemente para difundir la bioinformática y la biología computacional porque, como ellos mismos dicen, “el futuro llegó hace rato, pongan el agua para los fideos”.
Laboratorio de Fisiología de Proteínas (Departamento de Química Biológica)
QB9, 4to piso, Pabellón II, Teléfono: 4576-3300/09 interno 209
Dirección: Ignacio E. Sánchez y Diego U. Ferreiro
Integrantes: Pablo Manolo Rodríguez y Guido De Luca
Becario postdoctoral: Nicolás Palopoli
Tesistas de doctorado: R. Gonzalo Parra y Juliana Glavina
Tesistas de grado: Ezequiel G. Bos, Leandro G. Radusky y Franco Simonetti
VER LA OFERTA TECNOLÓGICA DE ESTE GRUPO EN LA WEB DE EXACTAS