Hallazgo para un 10
Un equipo de investigación de Exactas UBA, en el marco de una colaboración internacional, logró identificar genes que causan enfermedades de la hipófisis que provocan diferentes consecuencias como problemas de crecimiento, de visión, o malformación de paladar, entre otras. Este hallazgo, relacionado con la enfermedad que padece Lionel Messi, ayuda a reconocer el origen de la dolencia, ahorra peregrinación de médico en médico a los pacientes y establece un mejor diagnóstico para su tratamiento y posible evolución.
«Logramos identificar algunos genes nuevos como posibles causantes de deficiencias de la hipófisis junto a síndromes más severos», dice María Inés Pérez Millán, a cargo del Grupo de Genética Molecular en Endocrinología en el iB3 de Exactas UBA, quien sabe que este hallazgo ahorrará a los afectados y a sus familias peregrinaciones de médico en médico, numerosos estudios y no poca angustia. Así surge de los casi 150 casos pediátricos analizados provenientes de doce hospitales de todo el país. “Es la primera vez que se hace un estudio de estas dimensiones en Argentina, con esta cantidad de pacientes”, destaca Julián Martínez Mayer, primer autor de la investigación recién publicada en Journal of Clinical Endocrinology & Metabolism, y agrega: “A este logro se le suma, el porcentaje de afectados que al final de la secuenciación tienen un diagnóstico certero”.
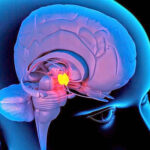
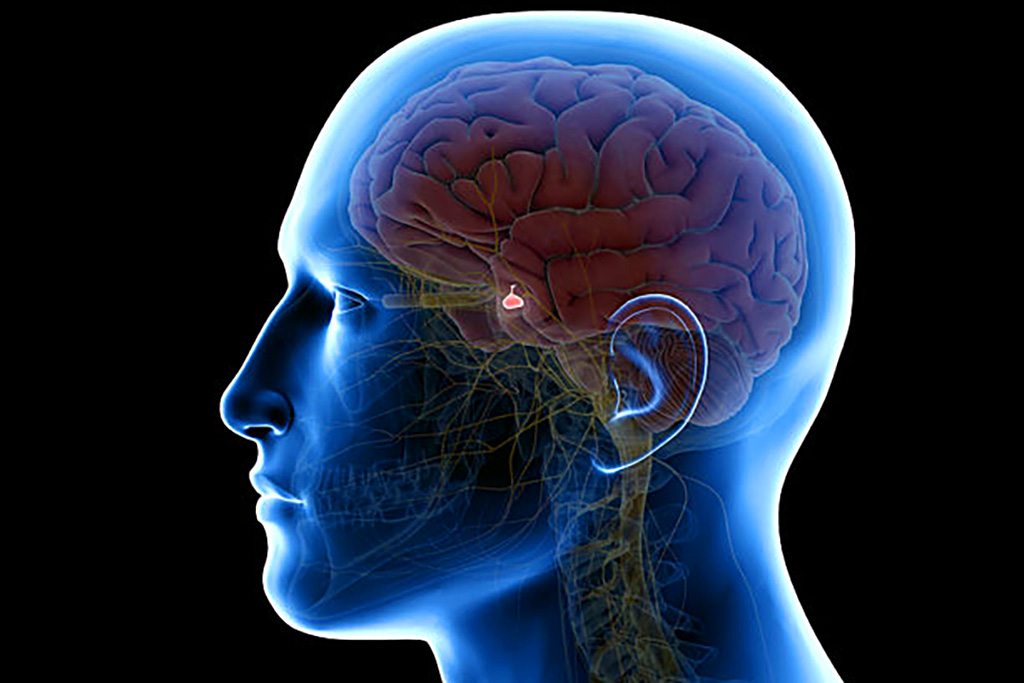
Hasta el momento, la forma habitual de detectar esta dolencia es por estudios clínicos dado que no abundaban demasiados datos de las causas genéticas del hipopituitarismo congénito, la disfunción endócrina pediátrica notificada con más frecuencia, con una incidencia de 1 cada 4 mil nacidos vivos. En estos casos, la hipófisis (también conocida como pituitaria) ubicada en el centro de la cabeza no produce cantidades normales de una, algunas o todas las hormonas que fabrica, claves para el crecimiento infantil, la pubertad y el metabolismo. Sus consecuencias son muy diversas según las hormonas afectadas y su grado de severidad.
A algunas personas les impide alcanzar una altura promedio de estatura y requieren hormona de crecimiento para mejorar su situación. Messi tiene esta enfermedad.
A algunas personas les impide alcanzar una altura promedio de estatura y requieren hormona de crecimiento para mejorar su situación. “Messi tiene esta enfermedad”, coinciden ambos científicos de Exactas UBA, quienes también destacan otras consecuencias según el caso: “La mayoría no desarrolla la pubertad de forma espontánea, sino que se induce con fármacos; también puede producir malformaciones en el paladar, en los rasgos faciales, problemas de visión, que pueden llevar a la ceguera; así como micropene o testículos pequeños”.
Cada caso es un mundo, y conocer con anticipación las características del trastorno permite tomar decisiones con mayor información. “Saber cuál es el gen que está causando la enfermedad, le permite al médico determinar qué seguimiento debe hacer. No siempre la presentación de la enfermedad es tan obvia, ni tan grave en un primer momento, sino que el paciente empieza a presentar síntomas a medida que va creciendo y cada vez más en mayor cantidad y complejidad”, indica Martínez Mayer. En este sentido, Pérez Millán, investigadora de CONICET, suma: “Es muy importante entender por qué le pasa lo que le pasa a tu hijo. Y planificar si se quiere tener más familia o no. O que esa persona que tiene la mutación cuando sea adulto sepa lo que tiene y conozca los riesgos que corre su descendencia”.
Hacerse los ratones
Hace años, el equipo del Instituto de Biociencia, Biotecnología y Biología Traslacional (iB3) en la Facultad de Ciencias Exactas y Naturales de la UBA, buscaba hurgar en las causas genéticas del hipopituitarismo, porque pensaban que sería “una buena idea para poder mejorar el diagnóstico de estos pacientes”, recuerdan.
El equipo decidió investigar si estos genes que producen una hipófisis con malformaciones en los ratones tienen alguna influencia en la enfermedad en los humanos.
Y apuntaron a la ciencia básica, en un proyecto que consiste en evaluar hipófisis dismórficas en diferentes ratones knockouts, desarrollados por un Consorcio Internacional de Fenotipado de Ratones (IMPC, en inglés). El objetivo de esta entidad es “deletear” cada uno de los genes del genoma de ratón por vez, para poder estudiar su función, al observar las consecuencias que provoca su ausencia.
“De las 209 líneas de ratones knockouts estudiadas, identificamos 51 que tienen malformaciones embrionarias de la hipófisis”, indica la investigación publicada en Genome Medicine.
El segundo paso fue aplicar los resultados de este estudio, a casi 150 pacientes con trastornos de esta enfermedad registrados en hospitales de todo el país, en Salta, Jujuy, CABA, Buenos Aires, La Plata, Córdoba, y Mendoza.
“Decidimos investigar si estos genes que producen una hipófisis con malformaciones en los ratones tienen alguna influencia en la enfermedad en los humanos. Y encontramos que sí, al menos en algunos casos”, resume el biólogo molecular Martínez Mayer.
De los 137 casos investigados el 19,1% y el 16% portaban variantes patógenas o probablemente patógenas en genes conocidos y nuevos.
En este sentido, la experta señala su importancia. “Fue un gran hallazgo. Se trató de dos genes que nunca antes los habíamos considerado en trastornos hipofisarios. Surgió a raíz del estudio de los ratones knockouts”, menciona la doctora en Biología, Pérez Millán, desde la Universidad de Michigan, en Estados Unidos, donde trabaja temporalmente para seguir investigando con estos roedores.
También en el exterior, en Alemania, y para una especialización, Martínez Mayer, precisa los datos obtenidos de la investigación con los pacientes de la Argentina. “De los 137 casos, -indica- el 19,1% y el 16% portaban variantes patógenas o probablemente patógenas en genes conocidos y nuevos, respectivamente; mientras que el 28,2% portaban variantes de significado incierto”. La conclusión señalada en el trabajo es contundente: “Estos resultados proporcionan una visión sin precedentes de la diversa etiología genética del hipopituitarismo”.
A futuro, sería posible que se vuelvan habituales escenarios ya registrados. Tal el caso de una familia que, a la hora de esperar su segundo bebe, sabía que, si padecía el mismo trastorno de su primera hija, podía correr riesgo de muerte a poco de nacer. “Secuenciamos al hermanito y tenía la misma variante genética de su hermana. Entonces, pudo ser medicado correctamente desde el primer momento, y eso cambia totalmente el panorama de su situación futura”, finaliza Pérez Millán.
Las dos investigaciones
En Journal of Clinical Endocrinology & Metabolism, se publicó bajo el título Exome Sequencing Has a High Diagnostic Rate in Sporadic Congenital Hypopituitarism and Reveals Novel Candidate Genes, el trabajo realizado por Julián Martínez Mayer, Sebastián Vishnopolska,Catalina Perticarari, Lucía Iglesias García, Martina Hackbartt, Marcela Martínez, Jonathan Zaiat, Andrea Jacome-Alvarado, Debora Braslavsky, Ana Keselman, Ignacio Bergadá, Roxana Marino, Pablo Ramírez, Natalia Pérez Garrido, Marta Ciaccio, María Isabel Di Palma, Alicia Belgorosky, María Verónica Forclaz, Gabriela Benzrihen, Silvia D’Amato, María Luján Cirigliano, Mirta Miras, Alejandra Paez Nuñez, Laura Castro, María Susana Mallea-Gil, Carolina Ballarino, Laura Latorre-Villacorta, Ana Clara Casiello, Claudia Hernández, Verónica Figueroa, Guillermo Alonso, Analía Morin, Zelmira Guntsche, Hane Lee, Eugene Lee, Yongjun Song, Marcelo Martí y María Inés Pérez Millán.
Y para el paper, Knockout mice with pituitary malformations help identify human cases of hypopituitarism, publicado en Genome Medicine los autores son Julián Martínez Mayer, Michelle Brinkmeier, Sean O’Connell, Arnold Ukagwu, Marcelo Marti, Mirta Miras, María Forclaz, María Benzrihen, Leonard Cheung, Sally A Camper, Buffy Ellsworth, Lori Raetzman, María Inés Pérez Millán y Shannon Davis.