Una proteína que inhibe la muerte celular
Investigadores dirigidos por Mario Galigniana estudian la regulación de la función biológica de proteínas pertenecientes a la familia de los receptores nucleares. Los estudios se centran en la función regulatoria de proteínas llamadas inmunofilinas, de alto peso molecular, que pueden inhibir la muerte celular programada.
En el Departamento de Química Biológica, un grupo de investigadores encabezados por el Dr. Mario Galigniana se dedica al estudio de la regulación de la función biológica de proteínas pertenecientes a la familia de los receptores nucleares. Fundamentalmente, se abocan a analizar a receptores de esteroides y factores de transcripción. En particular, los estudios están centrados en la función regulatoria que sobre todos ellos ejerce otro tipo de proteínas llamadas inmunofilinas de alto peso molecular.
“Las inmunofilinas de alto peso molecular fueron aisladas en asociación a los receptores de hormonas esteroides”, explica el Dr. Galigniana. Las hormonas esteroides son derivadas del colesterol y actúan como mensajeros químicos generando respuestas biológicas en las células cuando se unen a sus receptores específicos. Para entenderlo, puede usarse como analogía el funcionamiento de una antena (el receptor) con la señal de aire de la TV (la hormona) para generar la imagen (la respuesta biológica). Pero estos receptores no son proteínas aisladas sino que funcionan asociados a otras proteínas formando complejos. Una de las proteínas de ese complejo es la inmunofilina.
“Si bien son abundantes, la función biológica de las inmunofilinas es poco conocida”, reconoce el investigador, que fuera galardonado con una de las becas Guggenheim 2010. “Tuvimos la suerte de ser unos de los primeros en asignarle un rol funcional: participan del transporte y la relocalización subcelular de los receptores de esteroides”, agrega. Este hallazgo fue confirmado por otros laboratorios en el mundo y extendido a otros factores. Todos coinciden en afirmar que el hallazgo sugiere que podría ser un proceso relativamente general, ya que es compartido por otro tipo de proteínas que también están sujetas a relocalización dentro de la célula según los estímulos recibidos. “Hemos observado también que las inmunofilinas participan en la regulación de la actividad nuclear afectando la expresión de ciertos genes de la célula. Nos encontramos estudiando por qué ocurre esto y esperamos dilucidar el mecanismo en breve”, completa Galigniana.
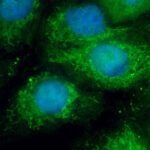
Una de las inmunofilinas analizadas por el grupo de investigación, la llamada FKBP51, se localiza primariamente en las mitocondrias de las células y, frente a diversos estímulos, es capaz de migrar al núcleo de manera reversible. Posteriormente, los investigadores demostraron que FKBP51 protege a las células de la muerte programada (apoptosis). “Pensamos entonces que, si esta proteína inhibe la muerte celular, era probable que participara en procesos tumorales”, explica Galigniana. Si la FKBP51 inhibe la apoptosis, podría actuar de esta manera cuando las células proliferan descontroladamente, en particular en procesos como el cáncer, escapando así a la regulación del programa de muerte celular que normalmente debería eliminarlas. Al estudiar varios tipos celulares tumorales, los investigadores vieron que la expresión de FKBP51 está aumentada en todos ellos. También comprobaron que si se inhibe su expresión, la célula se hace más sensible a la muerte. “Estudios subsecuentes con biopsias humanas demostraron que estas observaciones realizadas en líneas celulares tienen su correlato en los tejidos tumorales”, dice el investigador.
Actualmente, los investigadores están tratando de determinar si la medición del nivel de FKBP51 en plasma puede ser utilizada como marcador del pronóstico de la enfermedad, metástasis, sobrevida y remisión del cáncer. El equipo ha logrado obtener un anticuerpo monoclonal anti-FKBP51 que es útil para medir a la proteína de manera sensible. “Los resultados preliminares son promisorios, pero aún nos resta realizar un amplio muestreo con plasmas humanos para poder utilizarlo en estudios diagnósticos”, aclara Galigniana. Los estudios sobre el mecanismo de acción se están complementando al estudiar si FKBP51 ejerce un rol regulatorio sobre la actividad de otras proteínas que se relacionan con el control de ciclo de vida y muerte celular, como es el caso de varios factores transcripcionales y de una proteína esencial para mantener la estructura cromosómica luego de cada división de la célula.
Pero no toda la investigación sobre las inmunofilinas se relaciona con la proliferación celular y la apoptosis, también participan en el proceso de diferenciación celular del sistema nervioso. El equipo está estudiando la capacidad de las inmunofilinas FKBP51 y su prima-hermana, FKBP52, para regular la diferenciación neuronal a partir de células embrionarias, así como en el proceso de trans-diferenciación (es decir, la reprogramación de células ya comprometidas en un cierto linaje hacia otro diferente). Como consecuencia de estos estudios, también se están analizando a ambas immunofilinas como factores clave en el proceso de neurorregeneración luego de producido un daño en el tejido. “Los datos que poseemos hasta el momento son alentadores, estas proteínas son blancos terapéuticos para la regeneración de nervios seccionados y en modelos de daño de la columna vertebral”, afirma Galigniana.
Laboratorio de Bología Celular y Molecular (Departamento de Química Biológica)
4to piso, Pabellón II, Laboratorio QB68, teléfono 4576-3390 interno 215. E-mail: mgali@qb.fcen.uba.ar
Dirección: Mario Daniel Galigniana
Subgrupo de Receptores Nucleares: Dra. Alejandra Erlejman, Dra. Mariana Lagadari. Tesistas: Lic. Gisela Mazaira, Lic. Alejandro Molinari, Bioq. Ramiro Quinta, Lic. Cristina Daneri-Becerra, Lic. Luzia Ballmer.
Subgrupo de Oncología Molecular: Dr. Martin Monte, Dra. Fátima Ladelfa.
Tesistas: Lic. María Fernanda Toledo. Julieta Laiseca. Tesinista: Srta. Romina Cangelosi.