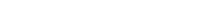
Las claves de la fábrica de energía celular
Científicos argentinos desentrañaron el mecanismo por el cual una proteína regula el proceso de fabricación, en el interior de las células, de la energía necesaria para la realización de las distintas funciones.
http://nexciencia.exactas.uba.ar/audio/DanielMurgida.mp3
Descargar archivo MP3 de Daniel Murgida
Todas las células, animales y vegetales, fabrican su propia energía a partir de nutrientes, como los hidratos de carbono, los lípidos y las proteínas. Esa energía se almacena en una molécula denominada adenosín trifosfato, más conocida como ATP. Mientras haya vida, hay producción de ATP. Y esa producción se asienta en una compleja maquinaria, cuya clave reside en la adecuada transferencia de electrones.
Las encargadas de transferir electrones son unas proteínas ancladas en las membranas de la célula, más precisamente, en la mitocondria, un compartimiento celular. Lo que no se sabía es cómo se regula esa maquinaria, tan compleja, para que los procesos ocurran con la dirección y la eficiencia necesarias.
Todas las reacciones químicas, en principio, pueden ocurrir en un sentido o en el contrario. “En estos sistemas, en particular, es muy alta la probabilidad de que una reacción química vuelva para atrás, por lo que pensamos que debería haber un mecanismo que regule muy finamente cómo se transfieren los electrones de un lugar a otro, que son el combustible para que ocurra la reacción”, señala Daniel Murgida, investigador del Instituto de Química Física de los Materiales, Medio Ambiente y Energía (INQUIMAE, UBA CONICET).
En efecto, el grupo que dirige Murgida demostró que existe un mecanismo muy sofisticado que regula, desde el punto de vista de la mecánica cuántica, la transferencia de electrones, para que sea realizada en una dirección adecuada. La clave reside en una proteína, denominada citocromo c oxidasa, que posee un sitio (átomos) de cobre, que participa de las reacciones de reducción y oxidación, o redox, nombre abreviado con que se designa a este tipo de reacciones.
Cabe aclarar que en toda reacción redox hay un elemento que cede electrones (agente reductor), y otro que los acepta (agente oxidante). El que pierde electrones, aumenta su estado de oxidación (se oxida). El agente oxidante, al captar electrones, se reduce, pues queda en un estado de oxidación inferior al que tenía.
En particular, para la producción del ATP –lo que se conoce como respiración celular–, las moléculas orgánicas de los nutrientes son degradadas mediante oxidación. Al final del proceso, el último en recibir electrones es el oxígeno molecular, que se reduce a agua.
Más lento, mejor
La célula podría realizar las reacciones de transferencia de electrones en un solo paso, de manera muy rápida, pero no serviría, porque esa reacción liberaría mucha energía en forma de calor. Sería algo equivalente a lo que sucede en un motor de combustión, que es muy ineficiente, si lo comparamos con un motor eléctrico, mucho más eficiente, o una lámpara de tungsteno frente a una lámpara de bajo consumo. Si la reacción que sucede en la mitocondria de la célula se realiza en un solo paso, estaría operando como la lamparita de tungsteno: desperdiciaría toda la energía para devolverla en forma de calor.
“Es necesario que ese proceso ocurra en forma muy regulada y, para eso, se necesita que las reacciones de transferencia electrónica múltiple que se van sucediendo estén muy bien direccionadas. De este modo, se logra que la reacción, aunque relativamente lenta, sea eficiente, y que el electrón no vuelva para atrás, porque, si vuelve, no genera el ATP”, detalla Murgida.
Los investigadores determinaron que el sitio de cobre de la proteína citocromo c oxidasa regula su tarea según un mecanismo de la física cuántica. “En particular–explica Murgida–, esa proteína tiene un centro de átomos de cobre, y es capaz de actuar como un hub [centro de operaciones], que puede recibir, con eficiencia, un electrón y desviarlo a 90 grados, también con mucha eficiencia, sin permitir que vuelva para atrás”.
El trabajo, que se publicó en la revista alemana Angewandte Chemie, fue realizado en colaboración con el grupo de Alejandro Vila, investigador del Instituto de Biología Molecular y Celular de Rosario (IBR, CONICET UNR). Los primeros autores fueron Ulises Zitare, becario doctoral del CONICET, y Damián Álvarez Paggi, ambos del INQUIMAE.
El mecanismo fue estudiado en el laboratorio mediante diversas técnicas, y los investigadores también recurrieron a la simulación por computadora, para ver cómo hace el sistema para desviar los electrones y transferirlos a larga distancia y con direccionalidad.
“Este mecanismo es interesante porque nos permite entender cómo se regula la respiración celular”, destaca Murgida, y prosigue: “Asimismo, aprendimos a regular distintos parámetros respecto de las propiedades redox de ese tipo de moléculas, y esto tiene posibles aplicaciones”.
En efecto, si es posible regular el potencial redox del centro de cobre y su afinidad por pequeñas moléculas que puede haber en el ambiente, se podría diseñar un sensor específico que detectara la presencia de determinados compuestos, por ejemplo, óxido nítrico.
La idea sería poder anclar esa proteína en un electrodo y hacerla trabajar como un sensor electroquímico. Otra posibilidad es que pueda funcionar como un catalizador eficiente, para acelerar alguna reacción de relevancia económica o industrial que, de otra forma, no se pueda producir con facilidad, como por ejemplo, la separación del agua en hidrógeno y oxígeno.
Mutaciones
Los investigadores lograron modificar la estructura de la proteína mediante mutaciones genéticas, y así pudieron generar cavidades que permitan que la sustancia que se quiera medir se una a los centros metálicos. También pudieron regular las propiedades electrónicas de esos centros para que entreguen electrones a ciertas especies y no a otras.
“La tercera aplicación interesante se vincula a la electrónica molecular, todo un campo muy nuevo de la física y la química, donde se busca, a largo plazo, generar circuitos electrónicos moleculares”, adelanta Murgida. En este caso, se reemplazarían los componentes, que hoy son de silicio, por biomoléculas. “Una molécula y no un sistema complejo actuaría como componente electrónico, como un transistor”, remarca Murgida.
El investigador concluye: “Si somos capaces de regular no sólo las ganas que tiene ese centro metálico de tomar o entregar un electrón, sino también la dirección y la velocidad con que lo hace, y además podemos encender y apagar esas ganas de tomar o ceder electrones, podremos diseñar un dispositivo electrónico a escala molecular”.
En resumen, se trata de una investigación básica que tiene un gran potencial de aplicación.